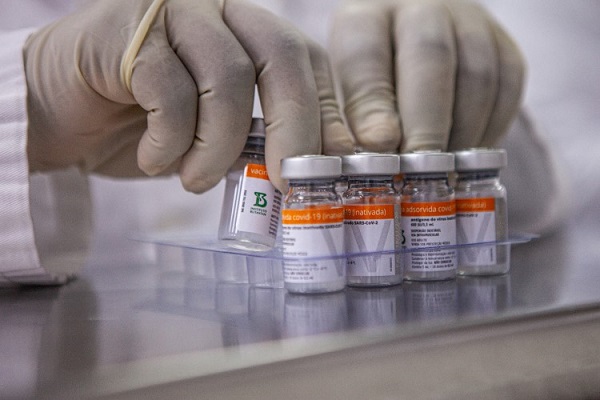
Rumo ao importante passo da imunização de crianças e adolescentes, a vacina Coronavac está emperrada na Agência Nacional de Vigilância Sanitária (Anvisa), uma vez que o Instituto Butantan afirma ter apresentado documentos necessários para a liberação, enquanto o órgão regulador nega que recebeu informações suficientes.
Conforme a Agência Folhapress, ainda na semana passada o Instituto anunciou a entrega de dados solicitados pela Anvisa, enquanto a Agência afirma que até ontem (15.nov.2021), o Butantan não havia entrado com novo pedido do uso da Coronavac para crianças e adolescentes.
Em 30 de julho o Butantan fez o primeiro pedido de autorização para o uso da Coronavac no público de 3 aos 17 anos. Essa solicitação foi negada pela Anvisa cerca de três semanas depois, em 18 de agosto, alegando que a mostra do estudo apresentado, com 586 participantes, era insuficiente e que não havia informações sobre os resultados de cada um dos subgrupos de faixas etárias, que compreende crianças de 3 a 5 anos; de 6 a 11 e de 12 a 17.
Ainda, técnicos da Anvisa apontaram a falta de dados sobre a eficácia em crianças com comorbidades ou com sistema imunológico debilitado, imunossuprimidas.
Da solicitação feita em agosta pela Anvisa, o Butantan disse que as informações foram apresentadas na reunião para os técnicos da Anvisa, que então pediram mais informações, entre elas as do último estágio das pesquisas antes que se obtenha o registro oficial na agência de vigilância, a chamada fase 3.
Vale ressaltar que, no caso da pandemia da Covid-19, para os maiores de 18 anos, as vacinas foram autorizadas em caráter emergencial, com os resultados da fase 2, no início de 2021. Além da Coronavac, o imunizante da Janssen também segue com esse mesmo caráter, enquanto Pfizer e AstraZeneca receberam autorização definitiva no Brasil.
A Coronavac é produzida no Brasil pelo Butantan, mas foi desenvolvida no laboratório chinês Sinovac, que anunciou na semana passada que dados preliminares de ensaios clínicos da fase 3, em crianças e adolescentes, feitos na África do Sul, no Chile, na Malásia e nas Filipinas, comprovaram a segurança para essa faixa etária.
Ainda, além da China, países como Chile, Equador e Indonésia já aprovaram a Coronavac para crianças e adolescentes e, segundo o laboratório chinês, não houve efeitos colaterais graves. Foram registradas reações de dor no local da injeção, dor de cabeça e febre.
Dimas Tadeu Covas, presidente do Butantan, defendeu, à Folha de S.Paulo, que a segurança e eficácia da Coronavac em crianças e adolescentes já está evidente com as pesquisas e aplicações em outros países.
"É muito importante para o Brasil que se aprove a Coronavac dos 3 aos 17 anos e não há mais razão para prorrogar essa decisão", argumentou.
Através da assessoria, a Anvisa afirmou que é necessário que o Instituto Butantan entre "com um pedido mais sólido e com as informações para esse público-alvo, para que a análise e os resultados tenham desfecho positivo".
Informou também que é necessário realizar o protocolo formal com o pedido de ampliação de uso da Coronavac em crianças e adolescentes. "Nesta petição o Butantan deve apresentar os estudos de eficácia e segurança para esses públicos, inclusive com os dados clínicos de fase 3", disse.
Foi confirmado pela Agência a reunião realizada com o Butantan. Segundo a Anvisa, houve uma "pré-submissão", com "uma apresentação de Power Point com uma breve descrição de dados", negando a exigência de novos documentos.
"Nessa reunião, a Anvisa identificou que faltavam informações para que fosse possível avançar para um pedido e posterior análise."
Em território nacional, o imunizante Pfizer é a única vacina contra o coronavírus que tem autorização da Anvisa para aplicação menores de 18 anos, apenas para aqueles que têm entre 12 e 17. Na última sexta-feira (12), a agência recebeu o pedido de uso desse imunizante em crianças de 5 a 11 anos. A solicitação deverá ser analisada em um prazo de até 30 dias.
Quanto à Coronavac, primeiro imunizante aplicado em solo nacional, uma nova reunião está marcada para acontecer na 6ª feira (19.nov.2021).